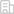國際微納生物領域權威期刊《Small》(影響因子13.3)報道了我校“微納生物技術”創新團隊孟濤教授的研究成果“Microbially Inspired Calcium Carbonate Precipitation Pathway Integrated Polyelectrolyte Capsules (MICPC) for Biomolecules Release”中文譯名:“受微生物啟發的整合碳酸鈣顆粒合成通路的聚電解質微囊(MICPC)用于緩釋生物分子”(DOI: 10.1002/smll.202306877)。論文第一作者為生命學院苑昊講師,通訊作者為孟濤教授,西南交通大學為第一署名單位。
聚電解質絡合,是指帶有相反電荷的聚電解質之間發生結合的過程,是合成微米、納米級藥物遞送載體的重要策略。在這個過程中,正電荷的聚電解質與負電荷的聚電解質之間相互吸引形成復合物。然而,由于電荷屏蔽效應,此復合物在生理環境中穩定性有限,從而導致基于聚電解質絡合策略形成的載體會突釋藥物,影響治療效果,限制了聚電解質復合物的潛在應用。受細菌通過尿素分解通路在其自身表面形成碳酸鈣顆粒的啟發,并基于本課題組近年來在全水相乳液以及催化領域的工作積累(ACS Applied Materials & Interfaces, 2022, 14, 4, 5009-5016;Chemical Engineering Journal, 2022, 454, 140276;Small Methods, 2022, 2201309),作者提出在聚電解質復合物中原位礦化產生碳酸鈣顆粒,以穩定聚電解質復合物,實現在生理環境中緩釋藥物(圖1)。結果顯示,相比于基于聚電解質絡合形成的微囊1天內突釋80%藥物,本研究提出的基于碳酸鈣顆粒的聚電解質微囊(MICPC)以每天3-10%的速率緩慢釋放藥物。并且,通過調控合成的碳酸鈣顆粒數量可對MICPC的釋放動力學進行精細調控。此外,MICPC通過生物相容的雙水相體系制備,可用于包封生物活性藥物并保持其活性,并可在生理環境中緩釋包封的藥物以治療相關疾病。在本研究中,MICPC用于包封及緩釋過氧化氫酶,且由于其自身攜帶負電荷可定植于帶有正電荷的炎癥部位,以有效清除細胞內活性氧及緩解炎癥。這項研究為聚電解質復合物在生理環境中的應用提供了通用策略,為生物藥物保存與遞送提供全新平臺。
圖1 受尿素分解細菌啟發,構建仿生礦化的聚電解質微囊MICPC(緩釋)及其與普通聚電解質微囊(突釋)在生理環境中釋放行為對比,且此MICPC可用于治療腸道炎癥疾病

本研究受到國家自然科學基金項目(22204130, 22378336, 21776230)、四川省科技廳項目(2021YFN0129, 2022NSFSC1211)、中央高校基礎研究基金(2682021ZTPY031, 2682023ZTPY048)的資助。
論文鏈接:https://onlinelibrary.wiley.com/doi/10.1002/smll.202306877