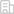臨床上,由于病原體與宿主之間復雜的相互作用,病毒-細菌混合肺炎會導致非常高的死亡率,對全世界人類健康造成了嚴重威脅。在新型冠狀病毒肺炎(COVID-19)全球大流行期間,幾乎所有嚴重的COVID-19患者都因繼發性細菌感染而接受抗生素治療,許多患者死于細菌繼發感染而非病毒本身,包括多重耐藥細菌感染。類似地,1918年流感病毒(H1N1)大流行期間,全球幾千萬死亡病例大部分是由細菌并發感染引起的。病毒-細菌混合性肺炎的高死亡率主要源于三個主要因素:1)病毒可以抑制對繼發性細菌感染的免疫反應。2)目前使用的幾乎所有安全劑量的抗生素都對多重耐藥細菌無效。3)長期的過度炎癥和過度活化的細胞因子會破壞宿主免疫系統。因此,迫切需要一種安全有效的治療策略,在根除病毒和細菌病原體的同時,不會導致過度炎癥引起的組織損傷,以達到治療病毒-細菌混合肺炎的目的。
篩選源自生物安全的天然材料的新型抗病毒和抗菌劑是擴大這種策略可能性的關鍵方法。中國自古就用中草藥治療各種疾病。然而,中草藥及其提取物在臨床實踐中的有限成功凸顯了研究其化學信息學和生物信息學的內在困難。具體而言,由復雜化學成分組成的中草藥及其提取物的藥理數據和藥物靶點不明確。此外,它們的治療效率和生物安全性仍有待進一步提高。
近期,Cell出版社旗下頂尖期刊Matter近期發表了天津大學材料科學與工程學院吳水林教授課題組及其合作團隊的一項最新研究成果“Material-herbology: An effective and safe strategyto eradicate lethal viral-bacterial pneumonia”,該團隊首次提出了中藥材料學的概念,通過材料學方法將中草藥處理成一種納米生物功能材料,以增強其治療效果。基于這一概念,在這項工作中,以中國茶為原料,該團隊提取了由多種兒茶素組成的天然茶納米點(TNDs,平均尺寸約為3 nm)。然后,作者探討了TNDs針對耐甲氧西林金黃色葡萄球菌(MRSA)的抗菌機制(跨膜相互作用和氨基酸的特定靶標)和針對H1N1流感病毒的抗病毒機制(抑制神經氨酸酶的活性位點)。該TNDs材料在小豬中具有優異的生物安全性。另外,在致死性H1N1-MRSA混合肺炎的小鼠模型治療中,TNDs與木犀草素結合后,采用霧化吸入治療比臨床報道的療法表現出更大的優勢,這是由于H1N1和MRSA的快速清除以及抗氧化相關的抗炎作用。
示意圖
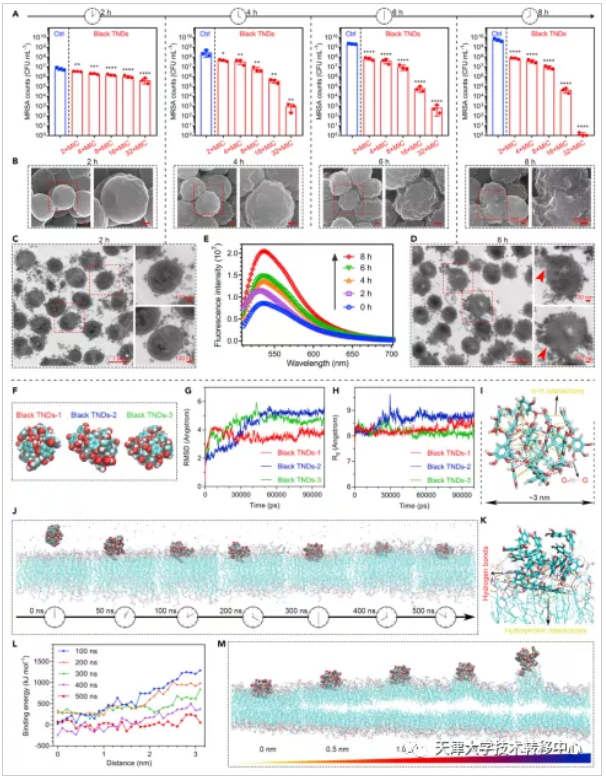
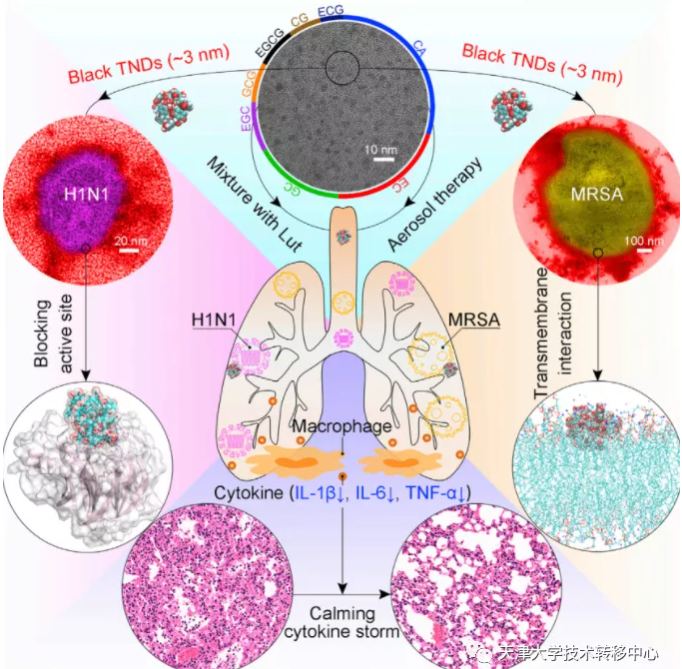
圖為抗菌表型和機制
首先,TNDs針對MRSA的抗菌表型和機制被研究。隨著時間的推移,TNDs會大量聚集在MRSA細菌表面,誘導MRSA膜逐漸滲透,破壞了整個膜結構從而殺滅細菌。TNDs與磷脂雙分子層之間的存在一定吸引作用,這種相互作用(氫鍵和疏水相互作用)確證了TNDs跨膜分子動力學模擬的順利完成。

圖為抗病毒表型和機制
然后,TNDs對H1N1病毒的抗病毒機制被研究。TNDs殺滅病毒時會吸附聚集在H1N1病毒表面。神經氨酸酶的活性位點處周圍的九個關鍵殘基充當氫鍵供體,能與TNDs之間形成大量的氫鍵相互作用。TNDs和H1N1病毒神經氨酸酶活性位點之間的密集氫鍵網絡能夠有效抑制H1N1病毒活性。
最后,通過藥物配伍篩選,TNDs和木犀草素具有最佳抗病毒和抗菌協同效果。在致死性H1N1-MRSA混合肺炎的小鼠模型治療中,TNDs與木犀草素結合后,采用霧化吸入治療比臨床報道的療法表現出更大的優勢,這是由于H1N1和MRSA的快速清除以及抗氧化相關的抗炎作用。
總之,這項工作描述了一種通過將TNDs與木犀草素結合來治療致死性H1N1-MRSA混合肺炎的中藥材料學策略。TNDs對MRSA的抗菌機制包括物理跨膜相互作用和抑制細菌氨基酸代謝,而針對H1N1的抗病毒機制是阻斷了病毒的神經氨酸酶活性位點。體內結果表明TNDs 在小豬中具有良好的生物安全性。在致死性H1N1-MRSA混合肺炎的小鼠模型治療中,TNDs與木犀草素結合后,采用霧化吸入治療比臨床報道的療法表現出更大的優勢,這是由于H1N1和MRSA的快速清除以及抗氧化相關的抗炎作用。因此,該中藥材料學策略可能為目前致死性細菌-病毒混合性肺炎的臨床治療帶來安全有效的替代方案。
吳水林教授課題小組專注于智能響應材料以及中藥材料學方法治療各類感染性疾病,只2017年以來,該團隊已經在Nature Communications, Science Advances, Advanced Materials, Journal of the American Chemical Society等知名期刊發表論文30多篇。